스위스 시장 진출
의료 기기 및 규제 프레임워크
CE 마크
(MDR/MedDO 또는 IVDR/IvDO 준수)
여정을 안내해 드립니다
- 제품 아이디어부터
- 개발까지
- 품질 시스템 구축
- 기술 문서 작성까지.
CE 마크와 그 이상의 가치를 실현하세요.
스위스 공인 대리점 (CH-REP)
당사는 귀사의 스위스 공인 대리인으로서 귀사를 대표합니다.
- 규정 준수 검토부터
- 등록까지
- 시장 감독 및 규제 인텔리전스
- 사고 처리까지.
스위스의 모든 것을 완벽하게 지원합니다.
왜 우리를 선택해야 할까요?
스위스 내 연락처
- >스위스에서 20년 이상의 실적. 우리는 우리 자신의 이름으로 서 있습니다.
- 스위스 내 잘 연결된 네트워크
- 스위스에 대한 규제 인텔리전스(EU, 미국, 호주 등 다른 시장도 가능)
- 강력한 전문가 품질, 규제 및 임상 배경
- 표준화된 CH-REP 프로세스
- 포괄적이고 투명한 비용
- 제품 책임 보험 가입 가능
- 순수한 CH-REP 기능: 경쟁 조항 없음
- 스위스메딕에 CH-REP로 정식 등록됨
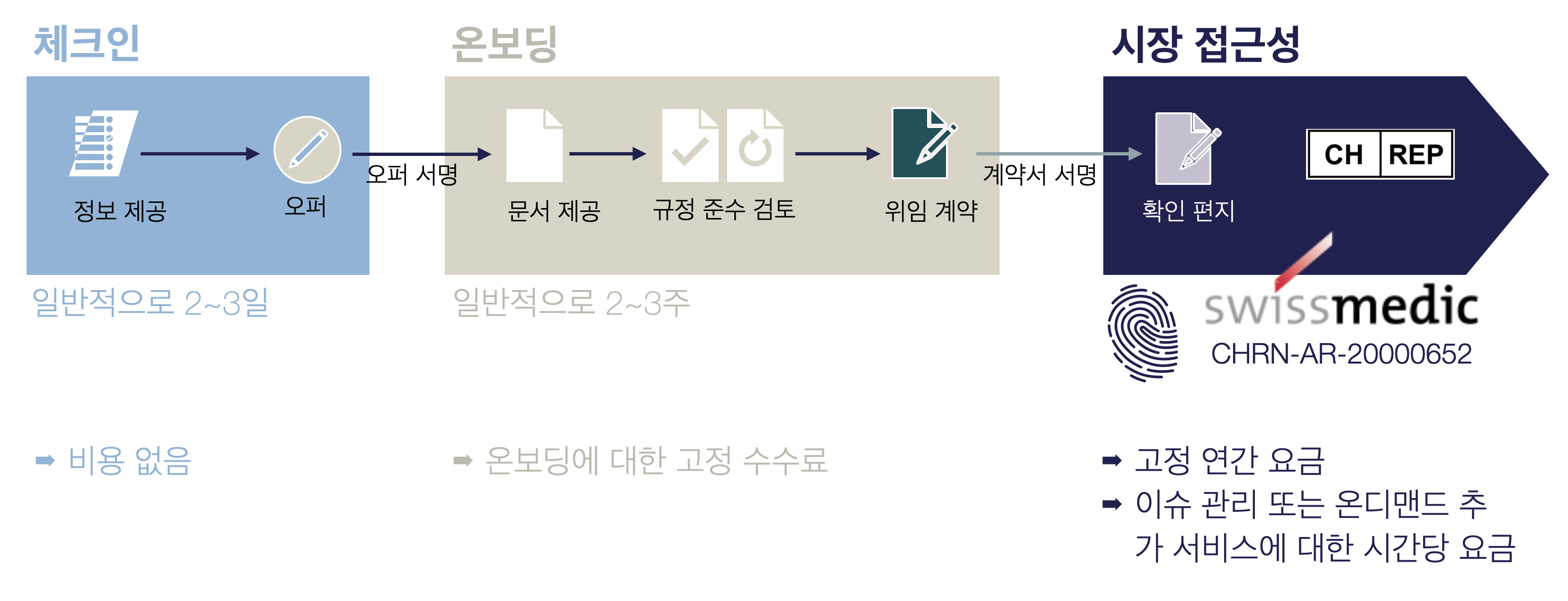
함께 일하기
CH-REP 온보딩 프로세스
고객 지원 방법
스위스 시장을 위한 의료 기기
- 스위스의 규제 환경에 대한 정기적인 업데이트
- 귀사의 제품에 맞는 맞춤형 지원
- 규정 준수 검토 및 갭 분석(ISO13485, MDSAP, MDR, IVDR, MedDO, IvDO, ISO9001)
- 경제 운영자 교육(제조업체, 수입업체, 유통업체, CH-REP, PRRC)
- 사고 처리
- Swissmedic, 인증 기관, 경제 운영자와의 커뮤니케이션.
- 기존 파트너로서 온디맨드 규제 자문 제공
- 스위스 내 네트워크 가속화
Get in Touch
Contact us for more information