スイスへの市場アクセス
医療機器と規制の枠組み
CEマーキング
(MDR/MedDOまたはIVDR/IvDOに準拠)
お客様の旅をガイドします
- 製品のアイデアから
- 開発
- 品質システムのセットアップ
- 技術文書作成まで
CEマーク取得、そしてその先へ。
スイス公認代表者 (CH-REP)
CH-REPとしてお客様の代理を務めます
- コンプライアンス審査から
- 登録まで
- 市場監視、規制情報
- インシデント対応まで
スイスのすべてをフルサポートします。
私たちを選ぶ理由
スイスでの連絡先
- >スイスで20年の実績。私たちは自らの名前を持っています。
- スイスにおけるネットワーク
- スイスの規制情報(EU、米国、オーストラリアなど他の市場も利用可能)
- 品質、規制、臨床に精通した専門家
- 標準化されたCH-REPプロセス
- 抑制された透明性の高いコスト
- 製造物責任保険が利用可能
- 純粋なCH-REP機能:競争条項なし
- CH-REPとしてSwissmedicに完全登録
私たちと一緒に働きましょう
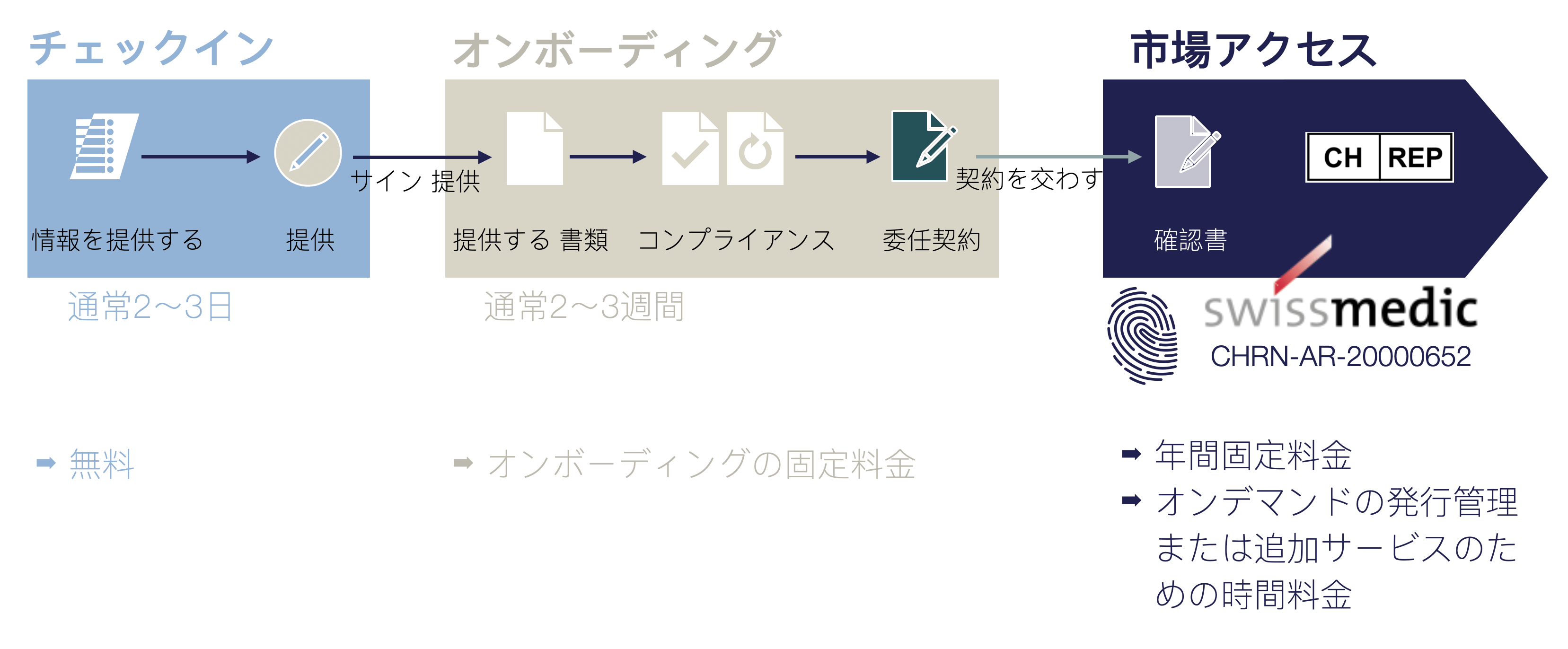
CH-REPのオンボーディング·プロセス
私たちのサポート
スイス市場向け医療機器
- スイスの規制に関する最新情報
- 貴社の製品に合わせたサポート
- コンプライアンスレビューとギャップ分析(ISO13485、MDSAP、MDR、IVDR、MedDO、IvDO、ISO9001)
- 経済事業者トレーニング(製造業者、輸入業者、流通業者、CH-REP、PRRC)
- インシデント対応
- スイスメディック、ノーティファイドボディ、経済事業者とのコミュニケーション
- 確立されたパートナーとしてのオンデマンド規制アドバイス
- スイス国内でのネットワーク促進
Get in Touch
Contact us for more information